
Licenciatura en Química
Yuliza Chavez - Katherin Rivera

TABLA PERIODICA
La tabla periódica de los elementos es una disposición de los elementos químicos en forma de tabla, ordenados por su número atómico, por su configuración de electrones y sus propiedades químicas.


Número Másico: Hace referencia a la suma de protones y neutrones que contiene el elemento
Número Atómico: Indica la cantidad de protones que presenta un átomo, que es igual a la de electrones
PRINCIPALES PROPIEDADES PERIODICAS
Son las características que tienen los elementos y que varían en forma secuencial por grupos y períodos
-
Estructura Electrónica: Distribución de los electrones en los orbitales del átomo. (Configuración electrónica)
-
Potencial de Ionización: Energía necesaria para arrancarte un electrón, en su estado fundamental de un átomo de un elemento en estado gaseoso


-
Electronegatividad: Es una medida que demuestra la capacidad que ostenta un átomo de atraer para si los electrones que corresponden a otro átomo cuando ambos conforman un enlace químico. Este enlace es un típico proceso químico a cargo de las interacciones que produce entre átomos, iones y moléculas


-
Afinidad Electrónica: Energía liberada para captar un electrón; es una medida de la variación de energía, cuando se añade un electrón a un átomo neutro para formar un ion negativo
-
Carácter Metálico: Define su comportamiento No metálico o Metálico. Un elemento se considera metal desde un punto de vista electrónico cuando cede fácilmente electrones y no tiene tendencia a ganarlos; es decir, los metales son muy poco electronegativos, un no metal es un elemento que difícilmente cede

-
Valencia iónica: Numero de electrones ganados o perdidos al formar un enlace iónico. Es la cantidad de electrones que son capaces de compartir los átomos de diversos elementos para formar un compuesto por medio de los enlaces iónicos. Es correcto hablar de valencias iónicas cuando se presenta la unión entre un elemento metálico y un elemento No metálico (Ley del Octeto)

-
Densidad: Es la relación entre la masa de un átomo y el volumen que este ocupa. Es una propiedad que depende del estado físico del elemento y la temperatura a la que se encuentre


-
Punto de Fusión: Es la temperatura a ala que el elemento cambia de la fase solidad a la liquido, igual a la presión de un átomo (atmosférica)
-
Punto de ebullición: Es la temperatura la cual la presión de vapor de un líquido es igual a la presión atmosférica


-
Calor específico: Es la cantidad de calor que se necesita por unidad de masa para elevar la temperatura un grado celsius. El calor especifico del agua es 1 caloría/gramo °C= 4,186 julios/gramo
-
Radio Atómico: Representa la distancia que existe entre el núcleo y la capa de valencia (la más externa). Por medio del radio atómico es posible determinar el tamaño del átomo dependiendo del tipo de elementos existentes diferentes técnicas para su determinación como la difracción de neutrones, de electrones o de rayos X.
-
En los grupos: el radio atómico aumenta con el numero atómico, es decir hacia abajo
-
En los periodos: Disminuye al aumento el número atómico, hacia la derecha, debido a la atracción que ejerce el núcleo sobre los electrones de los orbitales más externos, disminuyendo así la distancia núcleo – electrón.

-
Volumen Atómico: El volumen atómico fue definido por Meyer como el espacio que ocupa el átomo de un elemento y lo que calculo dividiendo la masa atómica del elemento entre su densidad, pero con un mismo elemento químico puede presentar varias estructuras solidas diferentes tendrá varios volúmenes.


-
Valencia Covalente: Número de electrones sin aparear que un átomo posee o puede poseer. En cada caso concreto la covalencia es el número de electrones de un átomo que forman enlaces
-
Numero de Oxidación: el número de oxidación de un átomo es un compuesto, es el número teórico (formal) que se obtiene aplicando unas reglas sencillas y que nos informan sobre la carga que presentaría dicho tomo, si los pares electrónicos que forman enlaces se asignaran a los átomos más electronegativos.

-
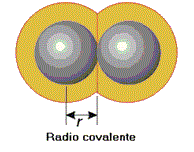
Radio covalente: es la mitad de la distancia entre dos núcleos de átomos iguales que están unidos mediante un enlace simple de una molécula neutra
-
Radio iónico: Es igual que el radio atómico, la distancia entre el centro del núcleo del átomo y del electrón establece más alejado del mismo, pero haciendo referencia no al átomo sino al ion


-
Estado de valencia: Es el número de electrones que le faltan o debe ceder un elemento químico para completar su ultimo nivel de energía
-
Peso atómico: es una cantidad física dimensional definida como la razón del promedio de las masas de los átomos de un elemento con respecto a la doceava parte de la masa de un átomo de carbono

-
Configuración electrónica: La configuración electrónica de un átomo de un elemento corresponde a la ubicación de los electrones en las orbitas de los diferentes niveles de energía

-
Símbolo químico: Son abreviaciones o signos que se utilizan para identificar los elementos y compuestos químicos
